�������ڣ�2023��11��29�� �Ķ���906
���ҩʦע�⣬һ����ҩ�Ƽ���˵������ˡ�
01��������ҩ�Ƽ���˵�����б�
11��22�գ�����ҩ�����վ�������������纮��ð������������ע��ҺҩƷ˵����Ĺ��桷�͡���������ʮ��ζɺ���Ƽ�ҩƷ˵����Ĺ��桷��
����ҩ��ֱ�ʾ������ҩƷ���������ɳ����˾�Ӧ�����ݡ�ҩƷע������취�����йع涨��������Ӧ����Ҫ����˵���飬�ڽ�������ǰ��ʡ��ҩƷ�ල�������ű������������漰ҩƷ��ǩ�ģ�Ӧ��һ��������;˵���鼰��ǩ��������Ӧ����ԭ������һ�¡��ڱ���֮����������ҩƷ�����ü���ʹ��ԭҩƷ˵���顣ҩƷ�������ɳ�����Ӧ���ڱ�����9�����ڶ��ѳ�����ҩƷ˵���鼰��ǩ���Ը�����
ͬʱ��ҩƷ�������ɳ�����Ӧ��������������Ӧ�������ƿ�չ�����о�����ȡ��Ч��ʩ����ҩƷʹ�úͰ�ȫ�������������ѵ��ָ��ҽʦ��ҩʦ���ߺ�����ҩ��
���⣬�ٴ�ҽʦ��ҩʦӦ����ϸ�Ķ�����ҩƷ˵����������ݣ���ѡ����ҩʱ��Ӧ����������˵������г�ֵĻ���/���շ���;������ҩǰӦ����ϸ�Ķ�ҩƷ˵���飬ʹ�ô���ҩ�ģ�Ӧ���ϸ���ҽ����ҩ��
�纮��ð����˵������Ҫ��
һ������ʾ���Ӧ�����ӣ�
��Ʒ����ƣ��˶�Ա���á�
���������ɡ���Ӧ�����ӣ�
�Ա�Ʒ�������ɷݹ����߽��á�
������������Ӧ����Ӧ�����ӣ�
�����ʾ���纮��ð�����ɼ����²�����Ӧ���棺
���ġ�Ż�¡��ڸɡ��ڿࡢ��к����ʹ����������;Ƥ�������ݡ����������ֲ�Ƥ����Ӧ;ͷ�Ρ���˯��ʧ�ߡ����������ơ��ļ¡�������Ӧ�ȡ�
�ġ���ע�������Ӧ�����ӣ�
��Ʒ���ʲݣ�����ͬʱ���ú��塢����ꪡ����ꪡ����졢ܾ�������Ƽ���
(ע����ԭ��˵����İ�ȫ�����ݽϱ���Ҫ�����ݸ�ȫ�����ϸ�ģ�Ӧ����ԭ�����ݡ�˵����������������������Ҫ��һ�µģ�Ӧ��һ����������)
������ע��Һ˵������Ҫ��
һ������ʾ���Ӧ�������������ݣ�
1.��Ʒ������Ӧ�����������ݿˣ�Ӧ����������������ҽ�ƻ���ʹ�ã�ʹ����Ӧ�����ܹ��������ݿ�������ѵ����ҩ����ֹ�����Ӧ���������ز�����Ӧ������ͣҩ����ʱ���Ρ�
2.��ֹ������ҩ��
������������Ӧ����Ӧ�������������ݣ�
���������ʾ����Ʒ�ɼ����²�����Ӧ��
������Ӧ��Ƥ�����졢Ƥ��������������ѡ��ļ¡��������������Ӧ���������ݿ˵ȡ�
ȫ�����ز����ʡ����ȵȡ�
Ƥ����Ƥ����֯��Ƥ��������ູ������ȡ�
��ϵͳ��ͷ�Ρ�ͷʹ�ȡ�
θ��ϵͳ�����ġ�Ż�¡���ʹ�ȡ�
�������ļ¡��������ѡ�ע�䲿λ��ʹ�ȡ�
���������ɡ���Ӧ�������������ݣ�
1.�Ա�Ʒ�������ɷݹ����߽��á�
2.��Ʒ�����״�����ֹ���ڶ�ͯ����ע�䡣
�ġ���ע�������Ӧ�������������ݣ�
1.��Ʒ������Ӧ�����������ݿˣ�Ӧ����������������ҽ�ƻ���ʹ�ã�ʹ����Ӧ�����ܹ��������ݿ�������ѵ����ҩ����ֹ�����Ӧ���������ز�����Ӧ������ͣҩ����ʱ���Ρ�
2.�ϸ���ҩƷ˵����涨�Ĺ�������ʹ�ã���ֹ������������ҩ��
3.�ϸ���ҩƷ˵�����Ƽ����÷�����ʹ�ã���ֹ������ҩ��
4.��ҩǰӦ����ϸѯ�ʻ����������ҩʷ����ʷ����ҩ�����ʷ��������������á�
5.��Ʒ���治�����ܻ�Ӱ��ҩƷ��������ҩǰӦ�������鱾Ʒ������ҩҺ���ֻ��ǡ���������ɫ���ᾧ��ҩ����״�ı��Լ�ƿ����©�������Ƶ�����ʱ��������ʹ�á�
6.�Ͻ�������飬����������ҩ����ƷӦ������ʹ�ã�����������ҩƷ�������ʹ�á�
7.�����ˡ����������쳣���ߵ�������Ⱥ�ͳ���ʹ����ҩע����Ļ���Ӧ������ʹ�ã���ǿ��⡣
8.��ǿ��ҩ�����ҩ�����У�Ӧ�����й۲���ҩ��Ӧ���ر��ǿ�ʼ30���ӡ������쳣������ͣҩ�����û������δ�ʩ�����λ��ߡ�
��ʮ��ζɺ���Ƽ�ҩƷ˵������Ҫ��
һ����������Ӧ����Ӧ�����ӣ�
���������ʾ�����Ƽ��ɼ����²�����Ӧ���棺���ġ�Ż�¡���к����ʹ���������ʡ�θ�����������ᡢƤ���������˯�����������ơ��ļµȡ�
���������ɡ���Ӧ�����ӣ�
1.�и��������ڸ�Ů���á�
2.�Ա�Ʒ�������ɷݹ����߽��á�
������ע�������Ӧ�����ӣ�
1.��ƷӦ����ҽ��ָ���°��涨�����ã������������ӷ������ͷ���ʱ�䡣
2.��ͯ���á�
3.���ظ������ܲ�ȫ���á�
4.��Ʒ��������������ͷ�����ҩ������ʹ�á�
(ע����ԭ��˵����İ�ȫ�����ݽϱ���Ҫ�����ݸ�ȫ�����ϸ�ģ�Ӧ������ԭ�����ݡ�˵����������������������Ҫ��һ�µģ�Ӧ��һ����������)
02����ҩ˵���������ϸ���ע������
��������������ҩ��ֶԶ���ҩƷ��˵����������������в���ҩƷ���г�ҩ����׳��ֹʹ���ҡ����ڹ�ͨ���ҵȣ��������±���
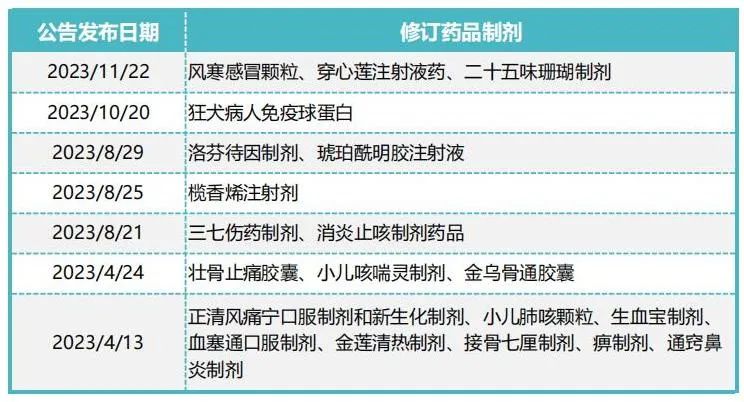
2023��2�£�����ҩ��ַ�������ҩע�����ר�Ź涨����Ҫ�������Ӧ����ǿ��ҩƷȫ�������ڵĹ�������ǿ��ȫ�Է��յļ�⡢���ۺͷ�����Ӧ��������ؼ���ָ��ԭ��ʱ����ҩ˵���顾���ɡ���������Ӧ����ע������������ơ������ر��ᵽ����ҩ˵���顾���ɡ���������Ӧ����ע��������κ�һ���ڱ��涨ʩ��֮����3�������ҩƷ��ע��ʱ��Ϊ���в���ȷ���ģ�����������ע�ᡣ
����ζ��3���ڣ�������ע�����ҩ���������ҩƷ������Ӧ�����ɺ�ע����������ݡ�
��ع涨����ҵ��˵���ܶ��ڻ������ʹ����Щ����֢��������Ӧ�Ȳ���ȷ��ҩ���Ͳ��������ˡ����Ǵӳ�Զ�������������ڴٽ��г�ҩ��ҵ���ԡ������ķ�չ��
���⣬�ϸ�ܿ�Ҳ��Դ���г�ҩ�������г��ľ�Ӱ��������OTCҩƷ�н��˳�Ϊ�г�ҩ������ҩ����˵����ع涨�ܹ����г�ҩ��˵������Ķ���ȫ����������Ȼ���������ҩ�İ�ȫ�ԣ��û��߶Ը���ҩƷ�γ�������
���α༭���� WWW.1168.TV 2023-11-29 11:35:12
������Դ����ҩ���ں�
1.������ע������Դ��1168ҽҩ����������������Ʒ����Ϊ���ݽ��ڻ������Ƽ�����˾-1168ҽҩ�������Ϸ�ӵ�а�Ȩ����Ȩʹ�õ���Ʒ��δ��������Ȩ����ת�ء�ժ�������������ʽʹ��������Ʒ���Ѿ�������Ȩʹ����Ʒ�ģ�Ӧ����Ȩ��Χ��ʹ�ã���ע������Դ��1168ҽҩ������http://www.1168.tv����Υ�����������ߣ�������������ط������Ρ�
2.����ת�ز�ע����������Դ����1168ҽҩ������������Ʒ��Ŀ�����ڴ��ݸ�����Ϣ����������������ͬ��۵��Ͷ�����ʵ�Ը��𣬲��е�������Ʒ��Ȩ��Ϊ��ֱ�����μ��������Ρ�
3.����ý�塢��վ����˴ӱ���ת��ʱ�����뱣������ע������Ʒ��һ��Դ�����Ը���Ȩ�ȷ������Ρ�
4.���漰��Ʒ���ݡ���Ȩ�����⣬������Ʒ����֮����һ�����뱾����ϵ��������Ϊ�������Ȩ������ϵ���䣺1753418380@qq.com��

�����÷�Χ�����ڻ��⾱���硢�����ȼ��պ�������֯��ʹ�����͵Ȳ���֢״��Ⱥ���������ʹ�÷��������á�����Ʒ����ֱ��ͿĨ�ڲ��ʲ�λ�����ᰴĦ2-3���ӣ�ÿ��2-3�Ρ�

�����÷�Χ�����ڻ��⾱���硢�����ȼ��պ�������֯��ʹ�����͵Ȳ���֢״��Ⱥ���������ʹ�÷��������á�����Ʒ����ֱ��ͿĨ�ڲ��ʲ�λ�����ᰴĦ2-3���ӣ�ÿ��2-3�Ρ�
 ���������� 44011102000390��
���������� 44011102000390��